La termodinámica del estado de agregado gaseoso de la materia es una rama importante de la física que estudia el equilibrio termodinámico y las transiciones cuasiestáticas en los sistemas. El modelo principal en el que se basan las predicciones del comportamiento de los sistemas es el modelo de gas ideal. Con su uso se obtuvo la ecuación de Mendeleev-Clapeyron. Considéralo en el artículo.
Gas ideal
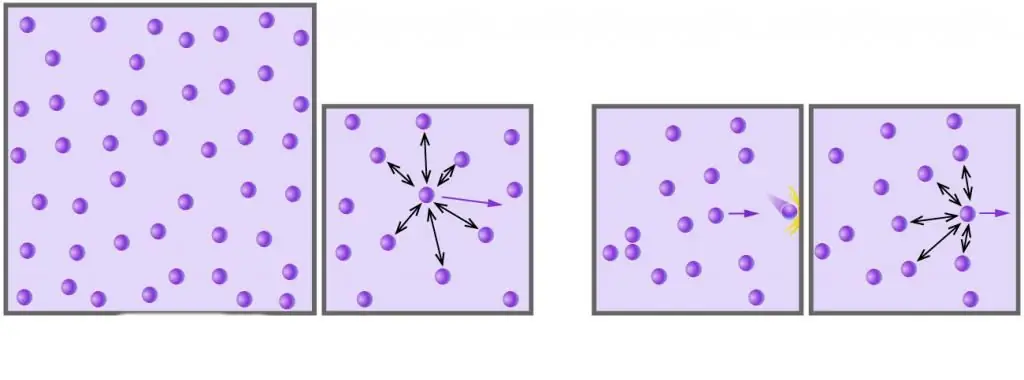
Como saben, todos los gases reales consisten en moléculas o átomos, cuyas distancias son demasiado grandes en comparación con su tamaño a bajas presiones. Además, a altas temperaturas, en escala absoluta, la energía cinética de las moléculas supera a su energía potencial asociada a interacciones dipolo-dipolo débiles (si además de estas interacciones existen otros tipos de enlaces químicos, por ejemplo, iónicos o hidrógeno, entonces hacen una contribución significativa al componente potencial de la energía interna del sistema).
Debido aPara muchos gases reales bajo condiciones cercanas a las normales, uno puede despreciar sus interacciones internas y tamaños de partículas. Estas dos aproximaciones principales constituyen el modelo de gas ideal.
Ecuación de Mendeleiev en física

Es más correcto y justo llamar a esta ecuación la ley de Clapeyron-Mendeleev. El caso es que fue registrado por primera vez por el ingeniero francés Emile Clapeyron en 1834. Lo hizo analizando las leyes de los gases de Boyle-Mariotte, Gay-Lussac y Charles descubiertas a principios del siglo XIX.
El mérito del químico ruso Dmitry Mendeleev radica en el hecho de que le dio a la ecuación una forma matemática moderna y fácil de usar. En particular, Mendeleev introdujo en la ecuación una constante para todos los gases R=8, 314 J/(molK). El propio Clapeyron utilizó una serie de constantes empíricas que dificultan el proceso de cálculo.
La ecuación de Mendeleev-Clapeyron se escribe de la siguiente manera:
PV=nRT.
Esta igualdad significa que el producto de la presión P y el volumen V en el lado izquierdo de la expresión siempre es proporcional al producto de la temperatura absoluta T y la cantidad de sustancia n en el lado izquierdo.
La expresión en estudio te permite obtener cualquier ley de los gases si fijas dos de sus cuatro parámetros. En el caso de los isoprocesos se estudian sistemas cerrados en los que no hay intercambio de materia con el medio (n=const). Estos procesos se caracterizan por un único parámetro termodinámico fijo (T, P o V).

Problema de ejemplo
Ahora resolvamos el problema en la ecuación de Mendeleev-Clapeyron. Se sabe que el oxígeno que pesa 500 gramos está en un cilindro con un volumen de 100 litros a una presión de 2 atmósferas. ¿Cuál es la temperatura en el globo, dado que el sistema está en equilibrio termodinámico?
Recuerde que, según la definición, la cantidad de una sustancia se calcula mediante la fórmula:
n=m/M.
Donde m es la masa de todas las partículas del sistema, M es su masa molar promedio. Esta igualdad nos permite reescribir la ecuación de Mendeleev de la siguiente forma:
PV=mRT/M.
Dónde obtenemos la fórmula de trabajo para esta tarea:
T=PVM/(mR).
Queda por convertir todas las cantidades a unidades SI y sustituirlas en esta expresión:
T=21013250, 10, 032/(0, 58, 314)=156 K.
La temperatura calculada es -117 oC. Aunque el oxígeno a esta temperatura sigue siendo gaseoso (se condensa a -182,96 oC), en tales condiciones, el modelo de gas ideal solo se puede utilizar para obtener una estimación cualitativa del valor calculado.






