El método conductimétrico de análisis es la medición de la conductividad electrolítica para monitorear el progreso de una reacción química. Esta ciencia se aplica ampliamente en química analítica, donde la titulación es un método estándar de operación. ¿Qué es la conductimetría? En la práctica común en química analítica, el término se usa como sinónimo de titulación, mientras que también se usa para describir aplicaciones que no son de titulación. ¿Cuál es el beneficio de usar este método de análisis? A menudo se usa para determinar la conductividad general de una solución o para analizar el punto final de una titulación que involucra iones.
Historia
Las mediciones conductivas comenzaron ya en el siglo XVIII, cuando Andreas Baumgartner notó que las aguas saladas y minerales de Bad Gastein enAustria conduce la electricidad. Por lo tanto, el uso de este método para determinar la pureza del agua, que a menudo se usa hoy en día para probar la efectividad de los sistemas de purificación de agua, comenzó en 1776. Así comenzó la historia del método conductimétrico de análisis.
Friedrich Kohlrausch continuó el desarrollo de esta ciencia en la década de 1860, cuando aplicó corriente alterna al agua, ácidos y otras soluciones. Alrededor de este tiempo, Willis Whitney, que estaba estudiando las interacciones de los complejos de ácido sulfúrico y sulfato de cromo, encontró el primer punto final conductimétrico. Estos hallazgos culminaron con la titulación potenciométrica y el primer instrumento para análisis volumétrico de Robert Behrend en 1883 en la titulación de cloruro y bromuro HgNO3. Por lo tanto, el método conductimétrico moderno de análisis se basa en Behrend.
Este desarrollo hizo posible probar la solubilidad de las sales y la concentración de iones de hidrógeno, así como valoraciones ácido-base y redox. El método conductimétrico de análisis se mejoró con el desarrollo del electrodo de vidrio, que comenzó en 1909.
Valoración
La titulación conductimétrica es una medida en la que la conductividad electrolítica de una mezcla de reacción se controla continuamente mediante la adición de un reactivo. El punto de equivalencia es el punto en el que la conductividad cambia repentinamente. Un aumento o disminución notable en la conductividad está asociado con un cambio en la concentración de los dos iones más conductivos, los iones de hidrógeno e hidróxido. Este métodose puede usar para valorar soluciones coloreadas o suspensiones homogéneas (p. ej., suspensión de pulpa de madera) que no se pueden usar con indicadores convencionales.
A menudo se realizan valoraciones ácido-base y redox, que utilizan indicadores comunes para determinar el punto final, como naranja de metilo, fenolftaleína para la valoración ácido-base y soluciones de almidón para un proceso redox de tipo yodométrico. Sin embargo, las mediciones de conductividad eléctrica también se pueden utilizar como herramienta para determinar el punto final, por ejemplo, al observar una solución de HCl con la base fuerte NaOH.
Neutralización de protones
A medida que avanza la valoración, los protones se neutralizan para formar NaOH formando agua. Por cada cantidad de NaOH añadida, se elimina un número equivalente de iones de hidrógeno. En efecto, el catión H+ móvil es reemplazado por el ion Na+ menos móvil, y la conductividad de la solución valorada, así como la conductividad celular medida, disminuyen. Esto continúa hasta que se alcanza un punto de equivalencia en el que se puede obtener una solución de cloruro de sodio NaCl. Si se agrega más base, hay un aumento a medida que se agregan más iones Na+ y OH- y la reacción de neutralización ya no elimina una cantidad apreciable de H+.

En consecuencia, cuando se titula un ácido fuerte con una base fuerte, la conductividad tiene un mínimo en el punto de equivalencia. este minimose puede usar en lugar de un colorante indicador para determinar el punto final de una titulación. La curva de valoración es un gráfico de valores medidos de conductividad o conductividad en función del volumen de solución de NaOH añadido. La curva de valoración se puede utilizar para determinar gráficamente el punto de equivalencia. El método conductimétrico de análisis (y su uso) es extremadamente relevante en la química moderna.
Reacción
Para una reacción entre un ácido débil y una base débil, la conductividad eléctrica primero disminuye un poco, ya que se utilizan pocos iones H+ disponibles. Entonces la conductividad aumenta ligeramente hasta el volumen del punto de equivalencia debido a la contribución del catión de la sal y del anión (esta contribución en el caso de una base ácida fuerte es despreciable y no se considera allí). Después de alcanzar el punto de equivalencia, la conductividad aumenta rápidamente debido a un exceso de iones OH.
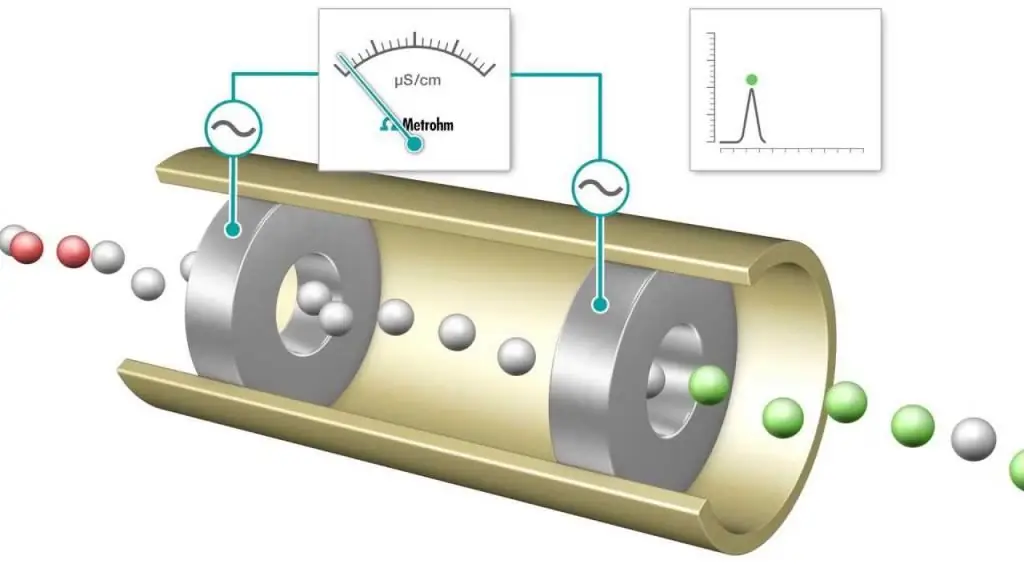
Los detectores de conductividad (método conductimétrico de análisis) también se utilizan para medir las concentraciones de electrolitos en soluciones acuosas. La concentración molar del analito que crea la conductividad de la solución se puede obtener a partir de la resistencia eléctrica medida de la solución.
Método conductimétrico de análisis: principio y fórmulas
(2.4.13) C=Constcell1Λm1Res, donde Constcell es un valor constante que depende de la celda de medida, Res es la resistencia eléctrica medida por el dispositivo (según la ley de Ohm Res=I / V, y con una constante tensión V medida I intensidad permite calcular Res), y Λm es el equivalenteconductividad para partículas iónicas. Aunque a efectos prácticos Λm puede considerarse constante, depende de la concentración según la ley de Kohlrausch:
(2.4.14)=Хт Λm0-ΘC, donde Θ es una constante y Λm0 es la conductividad molar límite característica de cada ion. La conductividad molar, a su vez, depende de la temperatura.
Escritura
El desarrollo del método conductimétrico de análisis de medidas ha llevado a los científicos a nuevos descubrimientos. Los científicos determinaron la relación de sobresaturación crítica, Scrit, usando conductimetría en un sistema homogéneo de precipitación de AgCl en exceso de iones Ag+, usando hidrólisis de cloruro de alquilo como fuente de iones de CI”. Encontraron Scrit=1.51, 1.73 y 1.85 a 15, 25 y 35°C respectivamente, donde S=([Ag+][Cl-] / Ksp) 1/2 por su definición. Si esta definición del factor de sobresaturación se convierte a la nuestra (S=[Ag+][Cl-] / Ksp), los resultados son 2,28, 2,99 y 3,42, respectivamente, en bastante buena concordancia con los resultados del presente estudio. Sin embargo, la dependencia de la temperatura de Scrit es opuesta a la descrita en el presente estudio. Aunque la razón de esta contradicción no está clara, la disminución de Scrit con el aumento de la temperatura puede ser bastante razonable, ya que la tasa de nucleación cambia drásticamente con un pequeño cambio en ΔGm/ kT y, por lo tanto, ΔGm/ kT, que es proporcional a T − 3 (lnSm) 2 según la fórmula (1.4.12) se considera casi constante con el cambio de temperatura en el sistema dado. Por cierto, la definición de S debe ser [Ag +] [Cl -] / Ksp, ya que la relación de sobresaturación en términos deLa concentración de monómero [AgCl] se da inicialmente como S=[AgCl] / [AgCl] (∞)=[Ag +] [Cl -] / Ksp.
Tanaka e Iwasaki
La historia del método conductimétrico de análisis fue continuada por dos icónicos científicos japoneses. Tanaka e Iwasaki estudiaron el proceso de nucleación de partículas de AgCl y AgBr utilizando el método de flujo detenido en combinación con un espectrofotómetro multicanal, que es útil para estudiar un proceso rápido del orden de mseg. Descubrieron que un complejo específico de haluro de plata AgXm (m-1), que tiene una banda de absorción UV bastante estrecha, se formaba instantáneamente cuando una solución de AgC104 del orden de 10-4 mol dm-3 se mezclaba con un KX (X=Cl o Br) solución del orden de 10-2 a 10-1 mol dm-3 seguido de su rápida descomposición de aproximadamente 10 ms con la formación de un producto intermedio que tiene una amplia absorción UV y un cambio mucho más lento en el espectro del producto intermedio. Interpretaron el intermedio como núcleos monodispersos (AgX) n que constaban de n moléculas y determinaron n a partir de la relación aparente -dC/dt α Cn en t=0 para varias concentraciones iniciales del precursor de C AgXm (m-1) - (n=7 -10 para AgCl, n=3-4 para AgBr).

Sin embargo, dado que el precursor AgXm (m − 1) se desintegra de manera no estacionaria, la teoría de la nucleación casi estacionaria no se aplica en este proceso y, por lo tanto, el valor resultante de n no corresponde al n valor de los núcleos críticos. Si el producto intermedio contiene núcleos monodispersos,formado por el complejo monomérico, es posible que no se mantenga la relación -dC/dt α C. A menos que supongamos que los grupos más pequeños que n-meros están en equilibrio, ki − 1, ici − 1c1=ki, i − 1ci, entre sí en una reacción secuencial c1 → c2 → c3 →… → cn − 1 → cn., y solo el último paso cn − 1 → cn es irreversible; es decir, c1⇌c2⇌c3⇌… ⇌cn − 1 → cn.
Además, se debe suponer que las concentraciones de los grupos de 2 a n-1 tienen concentraciones de equilibrio insignificantes. Sin embargo, no parece haber ninguna base para justificar estas suposiciones. Por otro lado, intentamos calcular los radios de los núcleos críticos y los coeficientes de sobresaturación S al final del proceso rápido, usando γ=101 mJ m − 2 para AgCl19 cúbico y γ=109 mJ m − 2 para AgBr20 cúbico, asumiendo que los valores de n, 7-10 para AgCl19 y 3-4 para AgBr20, son equivalentes al tamaño de núcleos monodispersos, n. El método conductimétrico de análisis, cuyas reseñas van desde la simple aprobación hasta la admiración, dio un nuevo nacimiento a la química como ciencia.
Como resultado, los científicos descubrieron la siguiente fórmula: r=0,451 nm y S=105 para AgCl con n=9; r=0.358 nm y S=1230 para AgBr con n=4. Ya que sus sistemas son comparables a los de Davis y Jones, que obtuvieron una sobresaturación crítica de AgCl de alrededor de 1.7-2.0 a 25 °C. Usando conductimetría de mezcla directa en volúmenes iguales de soluciones acuosas diluidas de AgNO3 y KCl, los valores de S extremadamente altos pueden no reflejar los factores de sobresaturación reales.en equilibrio con núcleos intermedios.
absorción UV
Parece más razonable atribuir un intermedio con amplia absorción UV a núcleos mucho más grandes que el promedio con una distribución de tamaño amplia generada por una reacción secuencial no estacionaria. El lento cambio posterior de los núcleos intermedios parece estar relacionado con su maduración en Ostwald.

En el contexto anterior, el químico estadounidense Nielsen también derivó un nsimilar alrededor de 12 y un S correspondiente mayor que 103 para la nucleación de partículas de sulfato de bario a partir de mediciones de turbidez en función de la sobresaturación, usando n=dlogJ / dlogC en una teoría similar a la de Becher-Dering a la fórmula. (1.3.37), pero dando (n + 1) en lugar de n. Dado que las soluciones de iones de bario e iones de sulfato se mezclaron directamente en este experimento, la nucleación transitoria rápida debería haber terminado inmediatamente después de la mezcla, y lo que se midió podría ser la tasa de maduración y/o fusión de Ostwald lenta posterior de los núcleos generados. Aparentemente, esta es la razón del valor irrazonablemente pequeño de n y la sobresaturación extremadamente alta. Por lo tanto, debemos señalar nuevamente que siempre es necesario algún reservorio de especies monoméricas que las libere en respuesta a su consumo para lograr la nucleación cuasi-estacionaria en un sistema cerrado. Todas las teorías clásicas de la nucleación, incluida la teoría de Becher-Döring, asumen implícitamente tal condición. Definición de conductimétricaEl método de análisis se proporcionó en las secciones del artículo anterior.
Otros científicos han investigado el proceso de nucleación transitoria de haluro de plata mediante radiólisis pulsada de agua que contiene haluro de metileno e iones de plata, durante la cual el haluro de metileno se descompone para liberar iones de haluro mediante electrones hidratados generados por radiación pulsada en el rango de 4 ns a 3 μs. Los espectros de los productos se registraron usando un fotomultiplicador y una cámara de rayas y se encontró que los precursores de haluro de plata monomérico se formaron durante un tiempo del orden de microsegundos seguido de un proceso de nucleación similar al observado por Tanaka e Iwasaki. Sus resultados muestran claramente que el proceso de nucleación de haluros de plata por mezcla directa de los reactivos consta de dos pasos elementales; es decir, la formación de un precursor monomérico del orden de μs y la posterior transición a núcleos del orden de 10 ms. Cabe señalar que el tamaño medio de los núcleos es de unos 10 nm.
Saturación
Con respecto a los coeficientes de sobresaturación para la nucleación de partículas de AgCl en sistemas abiertos en los que se introducen continuamente altas concentraciones de reactivos como AgNO3 y KCl en la solución de gelatina durante la precipitación, Strong y Wey31 informaron 1,029 (80 °C) - 1,260 (40 °C) y Leubner32 informaron 1,024 a 60 °C según lo estimado a partir de la medición de la tasa de crecimiento de las partículas de semillas de AgCl en sobresaturación crítica. Esta es la esencia del método conductimétrico de análisis cuantitativo.
Por otro lado, para sistemas abiertos de partículas de AgBr, algunosvalores estimados del coeficiente de sobresaturación crítica, Scrit: Scrit∼- 1,5 a 70 °C según Wey y Strong33 a partir de la tasa de crecimiento máxima dependiente del tamaño determinada al encontrar el umbral de renucleación a diferentes tasas de adición de una solución de AgNO3 a un KBr solución en presencia de partículas de semillas por los chorros dobles; Scrit=1,2-1,5 a 25 °C según Jagannathan y Wey34 como el factor de sobresaturación máximo determinado a partir de la ecuación de Gibbs-Thomson con sus datos sobre el tamaño promedio mínimo de los núcleos observados por microscopía electrónica durante el paso de nucleación de la precipitación de AgBr de dos chorros. Esto es muy efectivo cuando se aplica el método de cuantificación conductimétrica.

Al calcular estos valores de Scrit, tomaron γ=140 mJ m − 2. Dado que la nucleación en sistemas abiertos corresponde al proceso de supervivencia de los núcleos nacientes creados en una zona local de sobresaturación extremadamente alta cerca de las salidas de los reactivos, es fundamental la sobresaturación corresponde a la concentración del soluto en equilibrio con núcleos de tamaño máximo, si usamos los datos de Sugimoto35 sobre el radio máximo de núcleos de AgBr en sistemas abiertos (.3 8.3 nm) con γ teórico para AgBr cúbico (=109 mJ m − 2) 3, entonces el factor crítico de sobresaturación, Scrit, se calcula como 1,36 a 25 °C (si se supone que γ es 140 mJ/m2, entonces Scrit=1,48).
En consecuencia, en cualquier caso, las sobresaturaciones críticas enlos sistemas abiertos de partículas de haluro de plata suelen estar muy por debajo de las sobresaturaciones máximas (probablemente cercanas a las sobresaturaciones críticas) en los sistemas cerrados. Esto se debe a que el radio promedio de los núcleos generados en la zona local de un sistema abierto es mucho mayor que rm en un sistema cerrado, probablemente debido a la fusión instantánea de núcleos primarios altamente concentrados en la zona local de un sistema abierto con alta concentración local de electrolitos.
Solicitud
El uso del método de titulación conductimétrica para el registro continuo durante los procesos enzimáticos ha sido ampliamente estudiado y analizado. Casi todos los métodos analíticos electroquímicos se basan en reacciones electroquímicas (potenciometría, voltamperometría, amperometría, culombimetría).
El método conductimétrico de análisis es un método en el que no hay reacciones electroquímicas en los electrodos o hay reacciones secundarias que pueden despreciarse. Por lo tanto, en este método, la propiedad más importante de la solución electrolítica en la capa límite es su conductividad eléctrica, que varía de acuerdo con una amplia gama de reacciones biológicas.
Beneficios
Los biosensores conductimétricos también tienen algunas ventajas sobre otros tipos de transductores. En primer lugar, se pueden fabricar utilizando tecnología estándar de película fina de bajo coste. Esto, junto con el uso de un método optimizado para inmovilizar material biológico, conduce a una reducción significativa tanto en el costo primario de los dispositivos como encoste total del análisis. Para los microbiosensores incorporados, es fácil realizar el modo de medición diferencial, que compensa las influencias externas y mejora en gran medida la precisión de la medición.
Los datos muestran claramente el gran potencial de los biosensores conductimétricos. Sin embargo, esta sigue siendo una tendencia relativamente nueva en biosensores, por lo que el desarrollo de dispositivos comerciales tiene un futuro prometedor.
Nuevos métodos
Algunos científicos han descrito un método general para medir el pKa por conductancia. Este método fue ampliamente utilizado hasta alrededor de 1932 (antes de que se utilizaran los métodos de medición de pH). El método conductimétrico es extremadamente sensible a la temperatura y no se puede utilizar para medir valores de pKa superpuestos. Una posible ventaja para muestras sin cromóforo es que se puede utilizar en soluciones muy diluidas, hasta 2,8 × 10-5 M. En los últimos años se ha utilizado la conductimetría 87 para medir el pKa de la lidocaína, aunque el resultado obtenido fue de 0,7 por unidad por debajo del valor de pH generalmente aceptado.

Albert y Sergeant también describieron un método para determinar el pKa a partir de mediciones de solubilidad. Como se mencionó anteriormente, la solubilidad depende del pKa, por lo que si se mide la solubilidad en múltiples valores de pH en una curva, se puede determinar el pKa. Peck y Benet describieron un método general para estimar los valores de pKa para sustancias monopróticas, dipróticas y anfóteras dado un conjunto de medidas de solubilidad y pH. Hansen y Hafliger obtuvieron el pKa de la muestra, quese descompone rápidamente por hidrólisis a partir de sus velocidades de disolución iniciales en función del pH en un dispositivo de disco giratorio. El resultado concuerda bien con el resultado de pH/UV, pero la descomposición dificulta el último método. Esta es, en general, una descripción del método conductimétrico de análisis.






