El estado tridimensional del agua líquida es difícil de estudiar, pero se ha aprendido mucho analizando la estructura de los cristales de hielo. Cuatro átomos de oxígeno vecinos que interactúan con el hidrógeno ocupan los vértices de un tetraedro (tetra=cuatro, edro=plano). La energía promedio requerida para romper dicho enlace en el hielo se estima en 23 kJ/mol-1.

La capacidad de las moléculas de agua para formar un número dado de cadenas de hidrógeno, así como una fuerza dada, crea un punto de fusión inusualmente alto. Cuando se derrite, está retenido por agua líquida, cuya estructura es irregular. La mayoría de los enlaces de hidrógeno están distorsionados. Se necesita una gran cantidad de energía en forma de calor para romper la red cristalina del hielo unido por hidrógeno.
Características de la apariencia del hielo (Ih)
Muchos de los habitantes se preguntan qué tipo de red cristalina tiene el hielo. NecesarioCabe señalar que la densidad de la mayoría de las sustancias aumenta durante la congelación, cuando los movimientos moleculares se ralentizan y se forman cristales densamente empaquetados. La densidad del agua también aumenta a medida que se enfría hasta un máximo de 4°C (277K). Luego, cuando la temperatura cae por debajo de este valor, se expande.
Este aumento se debe a la formación de un cristal de hielo abierto con enlaces de hidrógeno con su red y menor densidad, en el que cada molécula de agua está rígidamente unida por el elemento anterior y otros cuatro valores, mientras se mueve lo suficientemente rápido como para tener mas masa. Desde que ocurre esta acción, el líquido se congela de arriba hacia abajo. Esto tiene importantes resultados biológicos, por lo que la capa de hielo del estanque aísla a los seres vivos del frío extremo. Además, dos propiedades adicionales del agua están relacionadas con sus características de hidrógeno: el calor específico y la evaporación.
Descripción detallada de estructuras
El primer criterio es la cantidad necesaria para elevar la temperatura de 1 gramo de una sustancia en 1°C. Elevar los grados del agua requiere una cantidad relativamente grande de calor porque cada molécula está involucrada en numerosos enlaces de hidrógeno que deben romperse para que la energía cinética aumente. Por cierto, la abundancia de H2O en las células y tejidos de todos los grandes organismos multicelulares significa que las fluctuaciones de temperatura dentro de las células se reducen al mínimo. Esta característica es crucial, ya que la velocidad de la mayoría de las reacciones bioquímicassensible.
El calor de vaporización del agua también es significativamente mayor que el de muchos otros líquidos. Se requiere una gran cantidad de calor para convertir este cuerpo en gas, porque los enlaces de hidrógeno deben romperse para que las moléculas de agua se disloquen entre sí y entren en dicha fase. Los cuerpos cambiantes son dipolos permanentes y pueden interactuar con otros compuestos similares y aquellos que se ionizan y disuelven.
Otras sustancias mencionadas anteriormente pueden entrar en contacto solo si existe polaridad. Es este compuesto el que está involucrado en la estructura de estos elementos. Además, puede alinearse alrededor de estas partículas formadas a partir de electrolitos, de modo que los átomos de oxígeno negativos de las moléculas de agua se orientan hacia los cationes, y los iones positivos y los átomos de hidrógeno se orientan hacia los aniones.
En los sólidos, por regla general, se forman redes cristalinas moleculares y atómicas. Es decir, si el yodo se construye de tal manera que contiene I2, , entonces en el dióxido de carbono sólido, es decir, en el hielo seco, las moléculas de CO2 son ubicado en los nodos de la red cristalina . Cuando interactúa con sustancias similares, el hielo tiene una red cristalina iónica. El grafito, por ejemplo, que tiene una estructura atómica basada en el carbono, no puede cambiarla, al igual que el diamante.
Qué sucede cuando un cristal de sal de mesa se disuelve en agua: las moléculas polares son atraídas por los elementos cargados del cristal, lo que conduce a la formación de partículas similares de sodio y cloruro en su superficie, lo que da como resultado estos cuerposse dislocan unos de otros, y comienza a disolverse. Desde aquí se puede observar que el hielo tiene una red cristalina con enlace iónico. Cada Na + disuelto atrae los extremos negativos de varias moléculas de agua, mientras que cada Cl - disuelto atrae los extremos positivos. La capa que rodea a cada ion se denomina esfera de escape y normalmente contiene varias capas de partículas de disolvente.
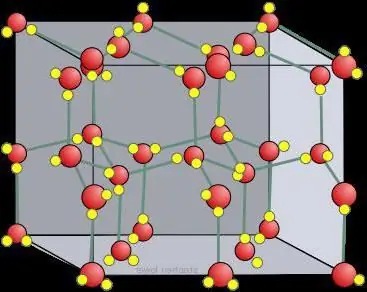
Rejilla de cristal de hielo seco
Se dice que las variables o un ion rodeado de elementos están sulfatados. Cuando el disolvente es agua, dichas partículas se hidratan. Así, cualquier molécula polar tiende a ser solvatada por los elementos del cuerpo líquido. En el hielo seco, el tipo de red cristalina forma enlaces atómicos en el estado de agregación, que no se modifican. Otra cosa es el hielo cristalino (agua congelada). Los compuestos orgánicos iónicos como la carboxilasa y las aminas protonadas deben ser solubles en grupos hidroxilo y carbonilo. Las partículas contenidas en tales estructuras se mueven entre las moléculas y sus sistemas polares forman enlaces de hidrógeno con este cuerpo.
Por supuesto, el número de los últimos grupos indicados en una molécula afecta su solubilidad, que también depende de la reacción de varias estructuras en el elemento: por ejemplo, los alcoholes de uno, dos y tres carbonos son miscibles con agua, pero los hidrocarburos más grandes con compuestos de un solo hidroxilo se diluyen mucho menos en líquidos.
Hexagonal Ih tiene una forma similar ared cristalina atómica. Para el hielo y toda la nieve natural en la Tierra, se ve exactamente así. Esto se evidencia por la simetría de la red cristalina de hielo, que crece a partir de vapor de agua (es decir, copos de nieve). Está en el grupo espacial P 63/mm de 194; D 6h, clase Laue 6/mm; similar a β-, que tiene un eje helicoidal múltiplo de 6 (rotación alrededor además de desplazamiento a lo largo de él). Tiene una estructura bastante abierta de baja densidad donde la eficiencia es baja (~1/3) en comparación con estructuras cúbicas simples (~1/2) o cúbicas centradas en las caras (~3/4).
En comparación con el hielo común, la red cristalina del hielo seco, unida por moléculas de CO2, es estática y cambia solo cuando los átomos se desintegran.
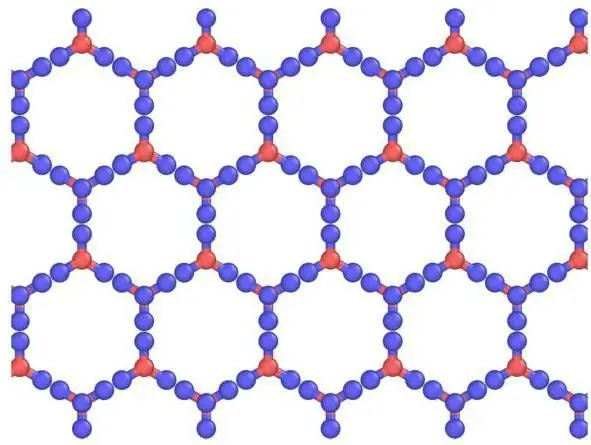
Descripción de las rejillas y sus elementos
Los cristales se pueden ver como modelos cristalinos, que consisten en láminas colocadas una encima de la otra. El enlace de hidrógeno está ordenado, mientras que en realidad es aleatorio, ya que los protones pueden moverse entre las moléculas de agua (hielo) a temperaturas superiores a unos 5 K. De hecho, es probable que los protones se comporten como un fluido cuántico en un flujo de túnel constante. Esto se ve reforzado por la dispersión de neutrones, que muestran su densidad de dispersión a medio camino entre los átomos de oxígeno, lo que indica localización y movimiento concertado. Aquí hay una similitud del hielo con una red cristalina molecular atómica.
Las moléculas tienen una disposición escalonada de la cadena de hidrógenocon respecto a sus tres vecinos en el plano. El cuarto elemento tiene una disposición de enlace de hidrógeno eclipsada. Hay una ligera desviación de la simetría hexagonal perfecta, ya que la celda unitaria es un 0,3% más corta en la dirección de esta cadena. Todas las moléculas experimentan los mismos entornos moleculares. Hay suficiente espacio dentro de cada "caja" para contener partículas de agua intersticial. Aunque generalmente no se consideran, recientemente se han detectado de manera efectiva mediante la difracción de neutrones de la red cristalina en polvo del hielo.
Sustancias cambiantes
El cuerpo hexagonal tiene puntos triples con agua líquida y gaseosa 0,01 °C, 612 Pa, elementos sólidos - tres -21,985 °C, 209,9 MPa, once y dos -199,8 °C, 70 MPa, así como - 34,7 °C, 212,9 MPa. La constante dieléctrica del hielo hexagonal es 97,5.
La curva de fusión de este elemento viene dada por MPa. Las ecuaciones de estado están disponibles, además de ellas, algunas desigualdades simples que relacionan el cambio en las propiedades físicas con la temperatura del hielo hexagonal y sus suspensiones acuosas. La dureza fluctúa con grados que van desde o por debajo del yeso (≦2) a 0 °C hasta el feldespato (6 Mohs) a -80 °C, un cambio anormalmente grande en la dureza absoluta (> 24 veces).
La red cristalina hexagonal del hielo forma placas y columnas hexagonales, donde las caras superior e inferior son los planos basales {0 0 0 1} con una entalpía de 5,57 μJ cm -2, y otras partes laterales equivalentes se llaman partes del prisma {1 0 -1 0} con 5, 94µJ cm -2. Se pueden formar superficies secundarias {1 1 -2 0} con 6.90 ΜJ ˣ cm -2 a lo largo de los planos formados por los lados de las estructuras.
Tal estructura muestra una disminución anómala de la conductividad térmica con el aumento de la presión (así como hielo cúbico y amorfo de baja densidad), pero difiere de la mayoría de los cristales. Esto se debe a un cambio en el enlace de hidrógeno, que reduce la velocidad transversal del sonido en la red cristalina de hielo y agua.
Existen métodos que describen cómo preparar grandes muestras de cristales y cualquier superficie de hielo deseada. Se supone que el enlace de hidrógeno en la superficie del cuerpo hexagonal bajo estudio estará más ordenado que dentro del sistema a granel. La espectroscopia variacional con generación de frecuencia de celosía de fase ha demostrado que existe una asimetría estructural entre las dos capas superiores (L1 y L2) en la cadena H2O del subsuelo de la superficie basal del hielo hexagonal. Los enlaces de hidrógeno adoptados en las capas superiores de los hexágonos (L1 O ··· HO L2) son más fuertes que los aceptados en la segunda capa a la acumulación superior (L1 OH ··· O L2). Estructuras de hielo hexagonales interactivas disponibles.
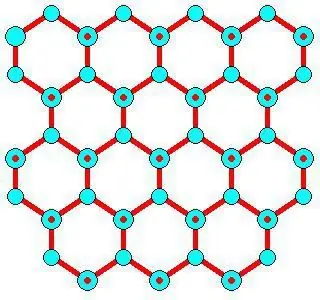
Características de desarrollo
El número mínimo de moléculas de agua necesarias para formar hielo es de aproximadamente 275 ± 25, como para un grupo icosaédrico completo de 280. La formación se produce a una velocidad de 10 10 en el interfaz aire-agua y no en agua a granel. El crecimiento de los cristales de hielo depende de diferentes tasas de crecimiento de variosenergías. El agua debe protegerse de la congelación cuando se criopreservan muestras biológicas, alimentos y órganos.
Esto generalmente se logra mediante velocidades de enfriamiento rápidas, utilizando muestras pequeñas y un crioconservador, y aumentando la presión para nuclear el hielo y evitar el daño celular. La energía libre del hielo/líquido aumenta de ~30 mJ/m2 a presión atmosférica a 40 mJ/m-2 a 200 MPa, lo que indica por lo que se produce este efecto.
¿Qué tipo de red cristalina es característica del hielo?
Alternativamente, pueden crecer más rápido a partir de superficies prismáticas (S2), en la superficie perturbada aleatoriamente de lagos agitados o congelados rápidamente. El crecimiento de las caras {1 1 -2 0} es al menos el mismo, pero las convierte en bases de prismas. Los datos sobre el desarrollo del cristal de hielo se han investigado a fondo. Las tasas de crecimiento relativas de elementos de diferentes caras dependen de la capacidad de formar un alto grado de hidratación conjunta. La temperatura (baja) del agua circundante determina el grado de ramificación en el cristal de hielo. El crecimiento de partículas está limitado por la tasa de difusión a un bajo grado de sobreenfriamiento, es decir, <2 °C, lo que da como resultado más de ellas.

Pero limitado por la cinética de desarrollo a niveles más altos de depresión de >4°C, lo que resulta en el crecimiento de agujas. Esta forma es similar a la estructura del hielo seco (tiene una red cristalina con una estructura hexagonal), varioscaracterísticas del desarrollo de la superficie y la temperatura del agua circundante (sobreenfriada), que está detrás de las formas planas de los copos de nieve.
La formación de hielo en la atmósfera afecta profundamente la formación y las propiedades de las nubes. Los feldespatos, que se encuentran en el polvo del desierto que ingresa a la atmósfera en millones de toneladas por año, son formadores importantes. Las simulaciones por computadora han demostrado que esto se debe a la nucleación de planos de cristales de hielo prismáticos en planos superficiales de alta energía.
Algunos otros elementos y celosías
Las sustancias disueltas (con la excepción de helio e hidrógeno muy pequeños, que pueden entrar en los intersticios) no pueden incluirse en la estructura Ih a presión atmosférica, sino que son forzadas a salir a la superficie o capa amorfa entre las partículas de la cuerpo microcristalino. Hay algunos otros elementos en los sitios de red del hielo seco: iones caotrópicos como NH4 + y Cl - que se incluyen en líquidos de congelación más ligeros que otros cosmotrópicos como Na + y SO42-, por lo que no es posible eliminarlos debido a que forman una fina película del líquido restante entre los cristales. Esto puede conducir a la carga eléctrica de la superficie debido a la disociación del agua superficial que equilibra las cargas restantes (lo que también puede provocar radiación magnética) y un cambio en el pH de las películas de líquido residual, por ejemplo, NH 42SO4 se vuelve más ácido y el NaCl se vuelve más básico.
Son perpendiculares a las carasred cristalina de hielo que muestra la siguiente capa unida (con átomos de O en negro). Se caracterizan por una superficie basal de crecimiento lento {0 0 0 1}, donde solo se unen moléculas de agua aisladas. Una superficie {1 0 -1 0} de rápido crecimiento de un prisma donde pares de partículas recién unidas pueden unirse entre sí con hidrógeno (un enlace de hidrógeno/dos moléculas de un elemento). La cara de más rápido crecimiento es {1 1 -2 0} (prismático secundario), donde las cadenas de partículas recién unidas pueden interactuar entre sí mediante enlaces de hidrógeno. Una de sus cadenas/molécula de elemento es una forma que forma crestas que dividen y fomentan la transformación en dos lados del prisma.
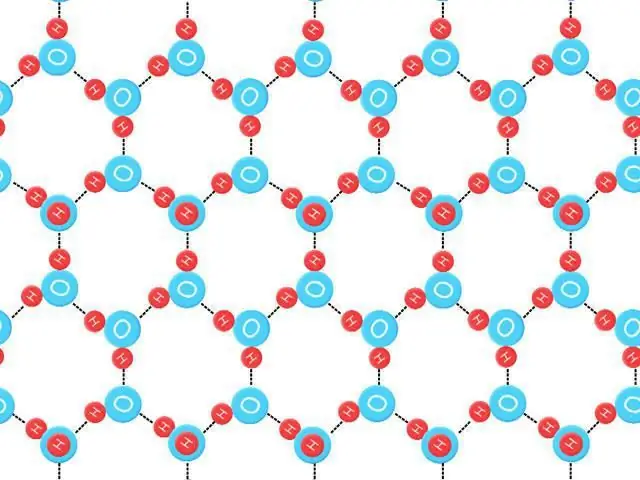
Entropía punto cero
Se puede definir como S 0=k B ˣ Ln (N E0), donde k B es la constante de Boltzmann, NE es el número de configuraciones en la energía E, y E0 es la energía más baja. Este valor para la entropía del hielo hexagonal en cero Kelvin no viola la tercera ley de la termodinámica "La entropía de un cristal ideal en el cero absoluto es exactamente cero", ya que estos elementos y partículas no son ideales, tienen enlaces de hidrógeno desordenados.
En este cuerpo, el enlace de hidrógeno es aleatorio y cambia rápidamente. Estas estructuras no son exactamente iguales en energía, pero se extienden a un gran número de estados energéticamente cercanos, obedecen las "reglas del hielo". La entropía de punto cero es el desorden que permanecería incluso si el material pudiera enfriarse hasta la temperatura absoluta.cero (0 K=-273, 15 ° C). Genera confusión experimental para el hielo hexagonal 3, 41 (± 0, 2) ˣ mol -1 ˣ K -1. Teóricamente, sería posible calcular la entropía cero de los cristales de hielo conocidos con mucha mayor precisión (despreciando los defectos y la dispersión del nivel de energía) que determinarla experimentalmente.
Los científicos y su trabajo en esta área
Se puede definir como S 0=k B ˣ Ln (N E0), donde k B es la constante de Boltzmann, NE es el número de configuraciones en la energía E, y E0 es la energía más baja. Este valor para la entropía del hielo hexagonal en cero Kelvin no viola la tercera ley de la termodinámica "La entropía de un cristal ideal en el cero absoluto es exactamente cero", ya que estos elementos y partículas no son ideales, tienen enlaces de hidrógeno desordenados.
En este cuerpo, el enlace de hidrógeno es aleatorio y cambia rápidamente. Estas estructuras no son exactamente iguales en energía, pero se extienden a un gran número de estados energéticamente cercanos, obedecen las "reglas del hielo". La entropía del punto cero es el desorden que permanecería incluso si el material pudiera enfriarse hasta el cero absoluto (0 K=-273,15 °C). Genera confusión experimental para el hielo hexagonal 3, 41 (± 0, 2) ˣ mol -1 ˣ K -1. Teóricamente, sería posible calcular la entropía cero de los cristales de hielo conocidos con mucha mayor precisión (despreciando los defectos y la dispersión del nivel de energía) que determinarla experimentalmente.

Aunque el orden de los protones en el hielo a granel no está ordenado, la superficie probablemente prefiera el orden de estas partículas en forma de bandas de átomos de H colgantes y pares simples de O (cero entropía con enlaces de hidrógeno ordenados). Se encuentra el desorden del punto cero ZPE, J ˣ mol -1 ˣ K -1 y otros. De todo lo anterior, es claro y comprensible qué tipos de redes cristalinas son características del hielo.






