La termodinámica es una rama importante de la física. Podemos decir con seguridad que sus logros han llevado al surgimiento de la era tecnológica y han determinado en gran medida el curso de la historia humana en los últimos 300 años. El artículo analiza la primera, segunda y tercera leyes de la termodinámica y su aplicación en la práctica.
¿Qué es la termodinámica?
Antes de formular las leyes de la termodinámica, averigüemos qué hace esta sección de la física.
La palabra "termodinámica" es de origen griego y significa "movimiento debido al calor". Es decir, esta rama de la física se dedica al estudio de cualquier proceso, como resultado del cual la energía térmica se convierte en movimiento mecánico y viceversa.
Las leyes básicas de la termodinámica se formularon a mediados del siglo XIX. La ciencia del "movimiento y el calor" considera el comportamiento de todo el sistema como un todo, estudiando el cambio en sus parámetros macroscópicos: temperatura, presión y volumen, y sin prestar atención a su estructura microscópica. Además, el primero de ellos juega un papel fundamental en la formulación de las leyes. Termodinámica en la física. Es curioso notar que se derivan únicamente de observaciones experimentales.
El concepto de un sistema termodinámico

Significa cualquier grupo de átomos, moléculas u otros elementos que se consideran como un todo. Las tres leyes están formuladas para el llamado sistema termodinámico. Algunos ejemplos son: la atmósfera de la Tierra, cualquier organismo vivo, la mezcla de gases en un motor de combustión interna, etc.
Todos los sistemas en termodinámica pertenecen a uno de los tres tipos:
- Abrir. Intercambian calor y materia con el medio ambiente. Por ejemplo, si la comida se cocina en una olla a fuego abierto, entonces este es un ejemplo vívido de un sistema abierto, ya que la olla recibe energía del ambiente externo (fuego), mientras que ella misma irradia energía en forma de calor. y el agua también se evapora de él (metabolismo).
- Cerrado. En tales sistemas no hay intercambio de materia con el medio ambiente, aunque se produce el intercambio de energía. Volviendo al caso anterior: si tapas la tetera con una tapa, puedes conseguir un sistema cerrado.
- Aislado. Este es un tipo de sistemas termodinámicos que no intercambian materia o energía con el espacio circundante. Un ejemplo sería un termo con té caliente.
Temperatura termodinámica

Este concepto significa la energía cinética de las partículas que forman los cuerpos circundantes, que refleja la velocidadmovimiento aleatorio de partículas. Cuanto más grande es, mayor es la temperatura. En consecuencia, al reducir la energía cinética del sistema, lo enfriamos.
Este concepto significa la energía cinética de las partículas que forman los cuerpos circundantes, que refleja la velocidad del movimiento caótico de las partículas. Cuanto más grande es, mayor es la temperatura. En consecuencia, al reducir la energía cinética del sistema, lo enfriamos.
La temperatura termodinámica se expresa en el SI (Sistema Internacional de Unidades) en Kelvin (en honor al científico británico William Kelvin, quien fue el primero en proponer esta escala). Comprender la primera, segunda y tercera leyes de la termodinámica es imposible sin una definición de temperatura.
Una división de un grado en la escala Kelvin también corresponde a un grado Celsius. La conversión entre estas unidades se realiza según la fórmula: TK =TC + 273, 15, donde TK y TC - temperaturas en grados Kelvin y Celsius respectivamente.
La peculiaridad de la escala Kelvin es que no tiene valores negativos. Cero en él (TC=-273, 15 oC) corresponde al estado en el que el movimiento térmico de las partículas del sistema está completamente ausente, parecen estar "congelados".
Conservación de la energía y la primera ley de la termodinámica

En 1824, Nicolas Léonard Sadi Carnot, un ingeniero y físico francés, hizo una sugerencia audaz que no solo condujo al desarrollo de la física, sino que también se convirtió en un paso importante en la mejora de la tecnología. Suse puede formular de la siguiente manera: "La energía no se crea ni se destruye, solo se puede transferir de un estado a otro".
De hecho, la frase de Sadi Carnot postula la ley de conservación de la energía, que formó la base de la 1ª ley de la termodinámica: "Siempre que un sistema recibe energía del exterior, la convierte en otras formas, la principal de que son térmicas y mecánicas."
La fórmula matemática de la primera ley se escribe de la siguiente manera:
Q=ΔU + A, aquí Q es la cantidad de calor transferido por el medio ambiente al sistema, ΔU es el cambio en la energía interna de este sistema, A es el trabajo mecánico perfecto.
Procesos adiabáticos
Un buen ejemplo de ellos es el movimiento de masas de aire a lo largo de las laderas de las montañas. Estas masas son enormes (kilómetros o más) y el aire es un excelente aislante térmico. Las propiedades anotadas nos permiten considerar como adiabático cualquier proceso con masas de aire que ocurra en un tiempo corto. Cuando el aire sube por la ladera de una montaña, su presión cae, se expande, es decir, realiza un trabajo mecánico y, como resultado, se enfría. Por el contrario, el movimiento descendente de la masa de aire va acompañado de un aumento de presión en la misma, se comprime y, por ello, se calienta mucho.
La aplicación de la ley de la termodinámica, que se discutió en el subtítulo anterior, se demuestra más fácilmente utilizando el ejemplo de un proceso adiabático.
Según la definición, como resultado de ella no hay intercambio de energía conambiente, es decir, en la ecuación anterior, Q=0. Esto conduce a la siguiente expresión: ΔU=-A. El signo menos aquí significa que el sistema realiza un trabajo mecánico al reducir su propia energía interna. Cabe recordar que la energía interna depende directamente de la temperatura del sistema.
Dirección de los procesos térmicos
Este número trata sobre la segunda ley de la termodinámica. Seguramente todos notaron que si pones en contacto dos objetos con diferentes temperaturas, el frío siempre se calentará y el caliente se enfriará. Tenga en cuenta que el proceso inverso puede ocurrir dentro del marco de la primera ley de la termodinámica, pero nunca se implementa en la práctica.
La razón de la irreversibilidad de este proceso (y de todos los procesos conocidos en el Universo) es la transición del sistema a un estado más probable. En el ejemplo considerado con el contacto de dos cuerpos de diferente temperatura, el estado más probable será aquel en el que todas las partículas del sistema tengan la misma energía cinética.
La segunda ley de la termodinámica se puede formular de la siguiente manera: "El calor nunca puede transferirse espontáneamente de un cuerpo frío a uno caliente". Si introducimos el concepto de entropía como una medida de desorden, entonces se puede representar de la siguiente manera: "Todo proceso termodinámico procede con un aumento de entropía".
Motor térmico

Este término se entiende como un sistema que, debido al suministro de energía externa al mismo, puede realizar un trabajo mecánico. PrimeroLas máquinas térmicas eran máquinas de vapor y se inventaron a finales del siglo XVII.
La segunda ley de la termodinámica juega un papel decisivo en la determinación de su eficacia. Sadi Carnot también estableció que la eficiencia máxima de este dispositivo es: Eficiencia=(T2 - T1)/T2, aquí T2 y T1 son las temperaturas del calentador y del refrigerador. El trabajo mecánico solo se puede realizar cuando hay un flujo de calor de un cuerpo caliente a uno frío, y este flujo no se puede convertir al 100% en energía útil.
La siguiente figura muestra el principio de funcionamiento de un motor térmico (Qabs - calor transferido a la máquina, Qced - pérdida de calor, W - trabajo útil, P y V - presión y volumen de gas en el pistón).
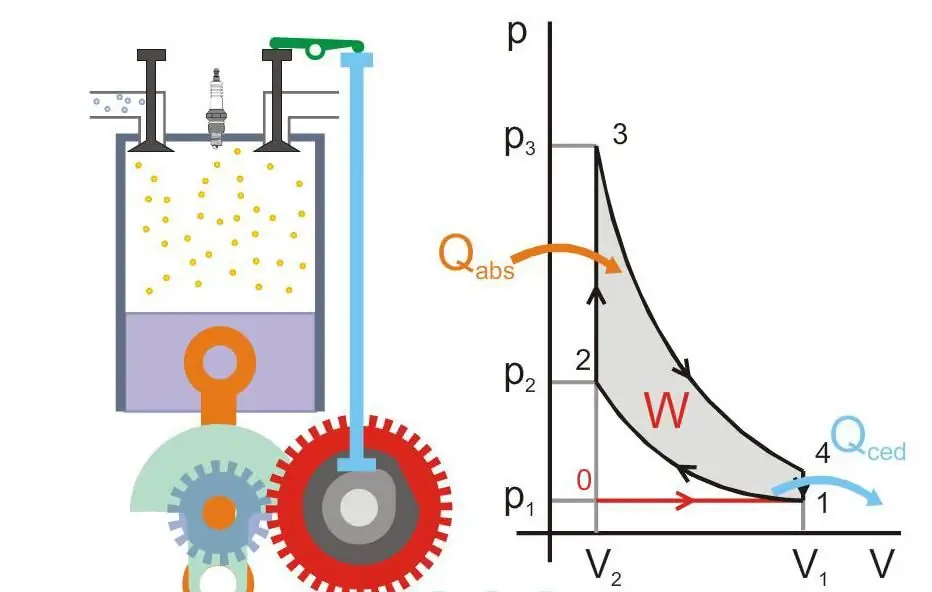
Cero absoluto y postulado de Nernst
Finalmente, pasemos a la consideración de la tercera ley de la termodinámica. También se le llama postulado de Nernst (el nombre del físico alemán que lo formuló por primera vez a principios del siglo XX). La ley dice: "El cero absoluto no se puede alcanzar con un número finito de procesos". Es decir, es imposible de ninguna manera "congelar" por completo las moléculas y los átomos de una sustancia. La razón de esto es el constante intercambio de calor existente con el medio ambiente.

Una conclusión útil extraída de la tercera ley de la termodinámica es que la entropía disminuye a medida que uno se acerca al cero absoluto. Esto significa que el sistema tiende a organizarse por sí mismo. Este hecho puedeutilizar, por ejemplo, para transferir paramagnetos a un estado ferromagnético cuando se enfrían.
Es interesante notar que la temperatura más baja que se ha alcanzado hasta ahora es 5·10−10 K (2003, laboratorio MIT, EE. UU.).






