Estudiar los procesos que ocurren en los sistemas estadísticos es complicado por el tamaño mínimo de las partículas y su enorme número. Es prácticamente imposible considerar cada partícula por separado, por lo tanto, se introducen cantidades estadísticas: la velocidad promedio de las partículas, su concentración, masa de partículas. La fórmula que caracteriza el estado del sistema, teniendo en cuenta parámetros microscópicos, se denomina ecuación básica de la teoría cinético-molecular de los gases (MKT).
Un poco sobre la velocidad promedio de las partículas
La determinación de la velocidad de las partículas se llevó a cabo por primera vez de forma experimental. Un conocido experimento del currículo escolar, realizado por Otto Stern, permitió crear una idea de las velocidades de las partículas. Durante el experimento, se estudió el movimiento de los átomos de plata en cilindros giratorios: primero, en un estado estacionario de la instalación, luego cuando giraba con una determinada velocidad angular.
Como resultado, se encontró que la velocidad de las moléculas de plata excede la velocidad del sonido y es de 500 m/s. El hecho es bastante interesante, ya que es difícil para una persona sentir tales velocidades de movimiento de las partículas en las sustancias.
Gas ideal
Continuar la investigaciónParece posible solo en un sistema cuyos parámetros pueden determinarse mediante mediciones directas utilizando instrumentos físicos. La velocidad se mide con un velocímetro, pero la idea de unir un velocímetro a una sola partícula es absurda. Solo se puede medir directamente un parámetro macroscópico asociado con el movimiento de las partículas.
Considere la presión del gas. La presión sobre las paredes del recipiente es creada por los impactos de las moléculas del gas en el recipiente. La peculiaridad del estado gaseoso de la materia está en distancias suficientemente grandes entre las partículas y su pequeña interacción entre sí. Esto le permite medir directamente su presión.
Cualquier sistema de cuerpos que interactúan se caracteriza por la energía potencial y la energía cinética del movimiento. El gas real es un sistema complejo. La variabilidad de la energía potencial no se presta a la sistematización. El problema se puede resolver introduciendo un modelo que tenga las propiedades características del gas, dejando de lado la complejidad de la interacción.
El gas ideal es un estado de la materia en el que la interacción de las partículas es insignificante, la energía potencial de interacción tiende a cero. Solo la energía del movimiento, que depende de la velocidad de las partículas, puede considerarse significativa.
Presión de gas ideal
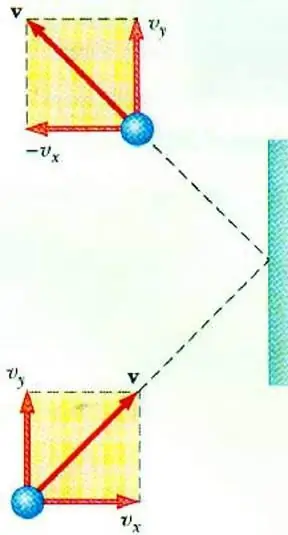
Revelar la relación entre la presión del gas y la velocidad de sus partículas permite la ecuación básica del MKT de un gas ideal. Una partícula que se mueve en un recipiente, al impactar con la pared, le transfiere un impulso, cuyo valor se puede determinar sobre la base de la segunda ley. Newton:
F∆t=2m0vx
El cambio en el momento de una partícula durante el impacto elástico está asociado con un cambio en el componente horizontal de su velocidad. F es la fuerza que actúa desde el lado de la partícula sobre la pared durante un corto tiempo t; m0 - masa de partículas.
Todas las partículas de gas chocan con la superficie del área S durante el tiempo ∆t, moviéndose en la dirección de la superficie con velocidad vx y ubicadas en un cilindro de volumen Sυ x Δt. A una concentración de partículas n, exactamente la mitad de las moléculas se mueven hacia la pared, la otra mitad se mueve en la dirección opuesta.
Habiendo considerado la colisión de todas las partículas, podemos escribir la ley de Newton para la fuerza que actúa sobre el área:
F∆t=nm0vx2S∆t
Dado que la presión del gas se define como la relación entre la fuerza que actúa perpendicular a la superficie y el área de esta última, podemos escribir:
p=F: S=nm0vx2
La relación resultante como ecuación básica del MKT no puede describir todo el sistema, ya que solo se considera una dirección de movimiento.
Distribución de Maxwell
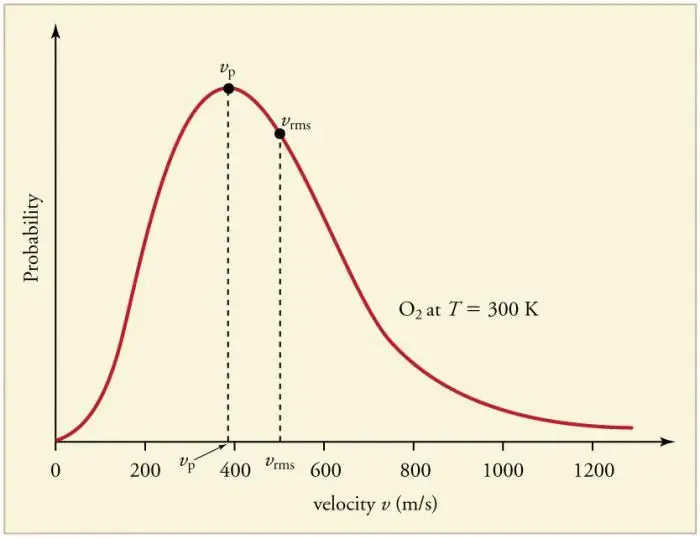
Las colisiones continuas y frecuentes de partículas de gas con las paredes y entre sí conducen al establecimiento de una cierta distribución estadística de partículas en términos de velocidades (energías). Las direcciones de todos los vectores de velocidad resultan igualmente probables. Esta distribución se llama distribución de Maxwell. En 1860 este patrón fuederivado por J. Maxwell sobre la base del MKT. Los principales parámetros de la ley de distribución se denominan velocidades: probable, correspondiente al valor máximo de la curva y raíz cuadrada media vkv=√‹v2 › - el cuadrado medio de la velocidad de la partícula.
El aumento de la temperatura del gas corresponde al aumento de la velocidad.
Basándonos en el hecho de que todas las velocidades son iguales y sus módulos tienen el mismo valor, podemos suponer:
‹v2›=‹vx2› + ‹v y2› + ‹vz2›, de: ‹ vx2›=‹v2›: 3
La ecuación básica del MKT, teniendo en cuenta el valor medio de la presión del gas, es:
p=nm0‹v2›: 3.
Esta relación es única porque determina la relación entre parámetros microscópicos: velocidad, masa de partículas, concentración de partículas y presión de gas en general.
Usando el concepto de la energía cinética de las partículas, la ecuación básica del MKT se puede reescribir de manera diferente:
p=2nm0‹v2›: 6=2n‹Ek›: 3
La presión de un gas es proporcional al valor medio de la energía cinética de sus partículas.
Temperatura
Curiosamente, para una cantidad constante de gas en un recipiente cerrado, uno puede relacionar la presión del gas y el valor promedio de la energía de movimiento de las partículas. En este caso, la presión se puede medir midiendo la energíapartículas.
¿Qué hacer? ¿Qué valor se puede comparar con la energía cinética? La temperatura resulta ser tal valor.

La temperatura es una medida del estado térmico de las sustancias. Para medirlo, se usa un termómetro, cuya base es la expansión térmica del fluido de trabajo (alcohol, mercurio) cuando se calienta. La escala del termómetro se crea experimentalmente. Por lo general, se colocan marcas en él correspondientes a la posición del fluido de trabajo durante algún proceso físico que ocurre en un estado térmico constante (agua hirviendo, hielo derretido). Diferentes termómetros tienen diferentes escalas. Por ejemplo, Celsius, Fahrenheit.

Escala de temperatura universal
Los termómetros de gas pueden considerarse más interesantes en términos de independencia de las propiedades del fluido de trabajo. Su escala no depende del tipo de gas utilizado. En un dispositivo de este tipo, se puede señalar hipotéticamente la temperatura a la que la presión del gas tiende a cero. Los cálculos muestran que este valor corresponde a -273,15 oC. La escala de temperatura (escala de temperatura absoluta o escala Kelvin) se introdujo en 1848. La posible temperatura de presión cero del gas se tomó como punto principal de esta escala. Un segmento unitario de la escala es igual a un valor unitario de la escala Celsius. Parece más conveniente escribir la ecuación MKT básica usando la temperatura cuando se estudian procesos de gas.
Relación entre presión y temperatura
Empiricamente, puedes verificar queproporcionalidad de la presión del gas a su temperatura. Al mismo tiempo, se encontró que la presión es directamente proporcional a la concentración de partículas:
P=nkT,
donde T es la temperatura absoluta, k es una constante igual a 1,38•10-23J/K.
El valor fundamental, que tiene un valor constante para todos los gases, se denomina constante de Boltzmann.
Comparando la dependencia de la presión con la temperatura y la ecuación básica de los gases MKT, podemos escribir:
‹Ek›=3kT: 2
El valor medio de la energía cinética del movimiento de las moléculas de un gas es proporcional a su temperatura. Es decir, la temperatura puede servir como medida de la energía cinética del movimiento de las partículas.






